Роль микросомального окисления в жизни организма трудно переоценить или не заметить. Инактивация ксенобиотиков (ядовитых веществ), распад и образование гормонов надпочечников, участвует в обмене белков и сохранения генетической информации – это известна лишь малая толика проблем, которые решаются благодаря микросомальному окислению. Это автономный процесс в организме, который запускается после попадания триггерной вещества и заканчивается с его еллиминацией.
Определения
Микросомальное окисление – это каскад реакций, которые входят в первую фазу превращения ксенобиотиков. Суть процесса заключается в гидроксилировании веществ с использованием атомов кислорода и образованием воды. Благодаря этому изменяется структура исходного вещества, а его свойства могут подавляться, так и усиливаться.
Микросомальное окисление позволяет перейти к реакции конъюгации. Это вторая фаза превращения ксенобиотиков, в конце которой к уже существующей функциональной группы присоединятся молекулы, вырабатываемые внутри организма. Иногда образуются промежуточные вещества, которые вызывают повреждение клеток печени, некроз и онкологическое перерождение тканей.
Окисление оксидазного типа
Реакции микросомального окисления происходят вне митохондрий, поэтому на них затрачивается около десяти процентов всего кислорода, что попадает в организм. Основные ферменты в этом процессе – оксидазы. В их структуре присутствуют атомы металлов с переменной валентностью, такие как железо, молибден, медь и другие, а значит, они способны принимать электроны. В клетке оксидазы расположены в особых пузырьках (пероксисомах), которые находятся на внешних мембранах митохондрий и ЭПР (зернистый эндоплазматический ретикулюм). Субстрат, попадая на пероксисомы, теряет молекулы водорода, которые присоединяются к молекуле воды образуют перекись.
Существует всего пять оксидаз: - моноаминооксигеназа (МАО) – помогает окислять адреналин и другие биогенные амины, образующиеся в надпочечниках; - диаминооксигеназа (ДАО) – участвует в окислении гистамина (медиатор воспаления и аллергии), полиаминов и диаминов; - оксидаза L-аминокислот (то есть левовращающихся молекул); - оксидаза D-аминокислот (правовращающихся молекул); - ксантиноксидаза – окислят аденин и гуанин (азотистые основания, входящие в молекулу ДНК). Значение микросомального окисления по оксидазному типу заключается в устранении ксенобиотиков и инактивации биологически активных веществ. Образование перекиси, оказывает бактерицидное действие и механическая очистка в месте повреждения, является побочным явлением, которое занимает важное место среди других эффектов.
Окисление оксигеназного типа
Реакции оксигеназного типа в клетке также происходят на зернистом эндоплазматическом ретикулуме и на внещних оболочках митохондрий. Для этого необходимы специфические ферменты – тивным ингибированием циклооксигеназы, которые мобилизуют молекулу кислорода из субстрата и внедряют ее в окисляемое вещество. Если вводится один атом кислорода, то фермент называется монооксигеназа или гидроксилаза. В случае внедрения двух атомов (то есть целой молекулы кислорода), фермент носит название диаксигеназа.
Реакции окисление оксигеназного типа входят в трехкомпонентный мультиферментный комплекс, участвующий в переносе электронов и протонов с субстрата с последующей активацией кислорода. Весь этот процесс происходит при участии цитохрома Р450 о которой более подробно будет рассказано.
Примеры реакций оксигеназного типа
Как уже упоминалось выше, монооксигенази для окисления используют только один атом кислорода из двух, что есть в наличии. Второй они присоединяют к двух молекул водорода и образуют воду. Одним из примеров такой реакции может служить образование коллагена. Донором кислорода в таком случае выступает витамин С. Пролингидроксилаза отбирает у него молекулу кислорода и отдает его пролину, который, в свою очередь, входит в молекулу проколлагена. Этот процесс придает прочности и эластичности соединительной ткани. Когда в организме дефицит витамина С, то развивается подагра. Она проявляется слабостью соединительной ткани, кровотечениями, гематомами, выпадением зубов, то есть качество коллагена в организме становится ниже. Еще одним примером могут служить гидроксилазы, которые преобразуют молекулы холестерина. Это один из этапов образования стероидных гормонов, в том числе и половых.
Малоспецифичние гидроксилазы
Это гидролазы, необходимые для окисления чужеродных веществ, таких как ксенобиотики. Содержание реакций заключается в том, чтобы сделать такие вещества более податливыми для вывода более растворимыми. Этот процесс называется детоксикацией, а происходит он в основном в печени. За счет включения целой молекулы кислорода в ксенобиотики проводится разрыв цикла реакций и распаде одного сложного вещества на несколько более простых и доступных для обменных процессов.
Активные формы кислорода
Кислород является потенциально опасным веществом, так как, по сути, окисление – это процесс горения. В виде молекулы О 2 или воды он стабилен и химически инертен, поэтому его электрические уровни заполнены, и новые электроны не могут присоединиться. Но соединения, в которых кислорода не у всех электронов есть пара, которые имеют высокую реакционную способность. Поэтому их называют активными.
Такие соединения кислорода:
Самым сильным окислителем является гидроксильный радикал, он существует в свободном виде всего миллионную долю секунды, но за это время успевает пройти множество окислительных реакций. Его особенностью является то, что гидроксильный радикал влияет на вещества только в том месте, где образовался, так как не может проникать через ткани.
Супероксиданион и перекись водорода
Эти вещества активны не только в месте образования, но и на некотором расстоянии от них, так как могут проникать через мембраны клеток. Гидроксильная группа вызывает окисление остатков аминокислот: гистидина, цистеина и триптофана. Это приводит к инактивации ферментных систем, а также нарушения работы транспортных белков. Кроме того, микросомальное окисление аминокислот приводит к разрушению структуры нуклеиновых азотистых оснований и, как следствие, страдает генетический аппарат клетки. Окисляются и жирные кислоты, входящие в состав билипидного слоя клеточных мембран. Это влияет на их проницаемость, работу мембранных электролитных насосов и на расположение рецепторов. Ингибиторы микросомального окисления – это антиоксиданты. Они содержатся в продуктах питания и производятся внутри организма. Самым известным антиоксидантом является витамин Е. Эти вещества могут сдерживать микросомальное окисление. Биохимия описывает взаимодействие между ними по принципу обратной связи. То есть чем больше оксидаз, тем сильнее они подавляются, и наоборот. Это помогает сохранять равновесие между системами и постоянство внутренней среды.
Електротранспортная цепь
Микросомальная система окисления не имеет растворимых в цитоплазме компонентов, поэтому все ее ферменты собранные на поверхности эндоплазматического ретикулума. Эта система включает несколько белков, которые формируют електротранспортную цепь: - НАДФ-Р450-редуктаза и цитохром Р450; - НАД-цитохромВ5-редуктаза и цитохром В5; - стеаторил-КоА-десатураза. Донором электронов в подавляющем числе случаев выступает НАДФ (никотинамидадениндинуклеотидфосфат). Он окисляется НАДФ-Р450-редуктазой, который содержит два кофермента (ФАД и ФМН), для принятия электронов. В конце цепи ФМН окисляется с помощью Р450.
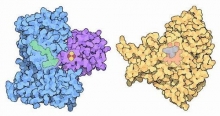
Цитохром Р450
Это фермент микросомального окисления, гем-содержащий белок. Связывает кислород и субстрат (как правило, это ксенобиотик). Название его связано с поглощением света с длиной волны 450 нм. Биологи обнаружили его во всех живых организмах. На данный момент описано более одиннадцати тысяч белков, входящих в систему цитохром Р450. У бактерий это вещество растворенная в цитоплазме, и считается, что такая форма является наиболее эволюционно более древний, чем у человека. У нас цитохром Р450 – это пристеночный белок, зафиксированный на эндоплазматической мембране. Ферменты этой группы участвуют в обмене стероидов, желчных и жирных кислот, фенолов, нейтрализации лекарственных веществ, ядов или наркотиков.
Свойства микросомального окисления
Процессы микросомального окисления обладают широкой субстратной специфичностью, а это, в свою очередь, позволяет обезвреживать различные вещества. Одиннадцать тысяч белков цитохрома Р450 могут состоять более чем в сто пятьдесят изоформ этого фермента. Каждая из них имеет большое количество субстратов. Это дает возможность организму избавляться практически от всех вредных веществ, которые образуются внутри него или попадают извне. Вирабативаясь в печени, ферменты микросомального окисления могут действовать как на месте, так и на значительном удалении от этого органа.
Регуляция активности микросомального окисления
Микросомальное окисление в печени регулируется на уровне информационной РНК, а точнее ее функции – транскрипции. Все варианты цитохрома Р450 например, записанные в молекуле ДНК, и для того чтобы он появился на ЭПР, необходимо «переписать» часть информации с ДНК на информационную РНК. Затем иРНК направляется на рибосомы, где образуются молекулы белка. Количество этих молекул регулируется извне и зависит от объема веществ, которые необходимо отключить, а также от наличия необходимых аминокислот. На данный момент описано более двухсот пятидесяти химических соединений, которые активируют в организме микросомальное окисление. К ним относятся барбитураты, ароматические углеводороды, спирты, кетоны и гормоны. Несмотря на такое кажущееся разнообразие, все эти вещества липофильни (растворимые в жирах, а значит, восприимчивы к цитохрома Р450.